

Sponsored Link
水素結合と疎水性相互作用
前回の双極子とファンデルワールス力ではファンデルワールス力について見ました。今回は残りの水素結合や疎水性相互作用について見ていきたいと思います。
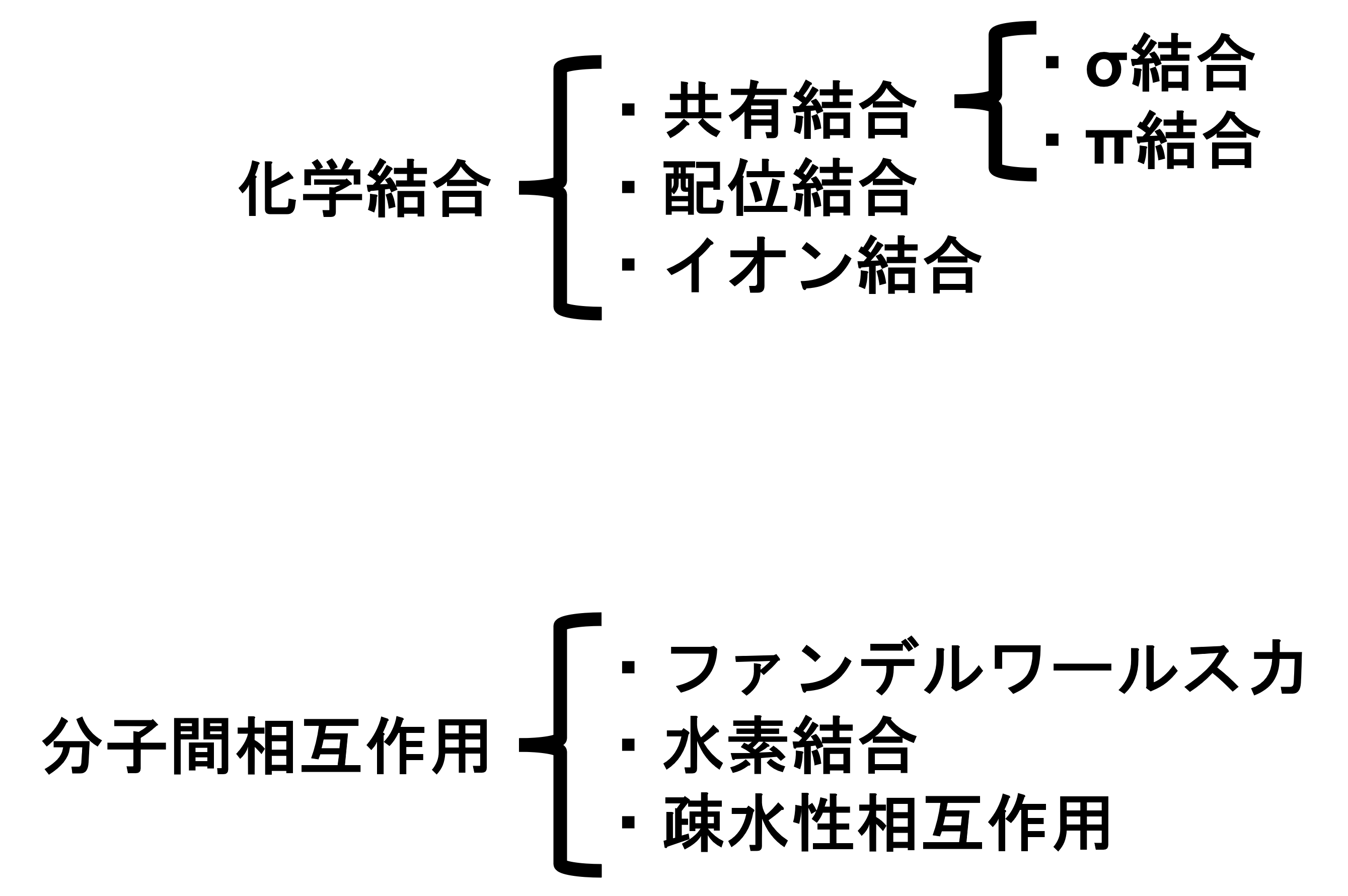
水素結合
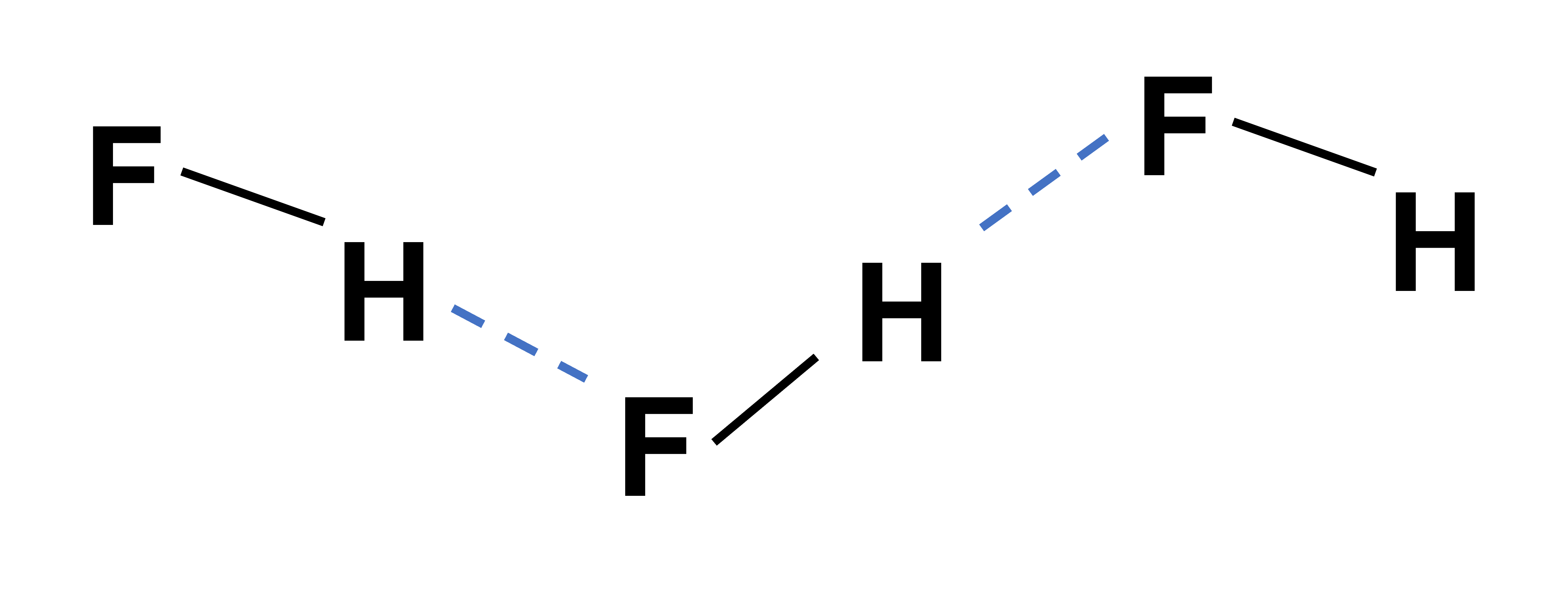
電気陰性度が大きいフッ素F、酸素O、窒素Nなどに直接ついて電子をとられた水素Hと、他の分子や分子内にあるF、O、Nなどの原子間に働く相互作用を水素結合と言います。例えばフッ化水素HFは以下のように水素結合が作られます。
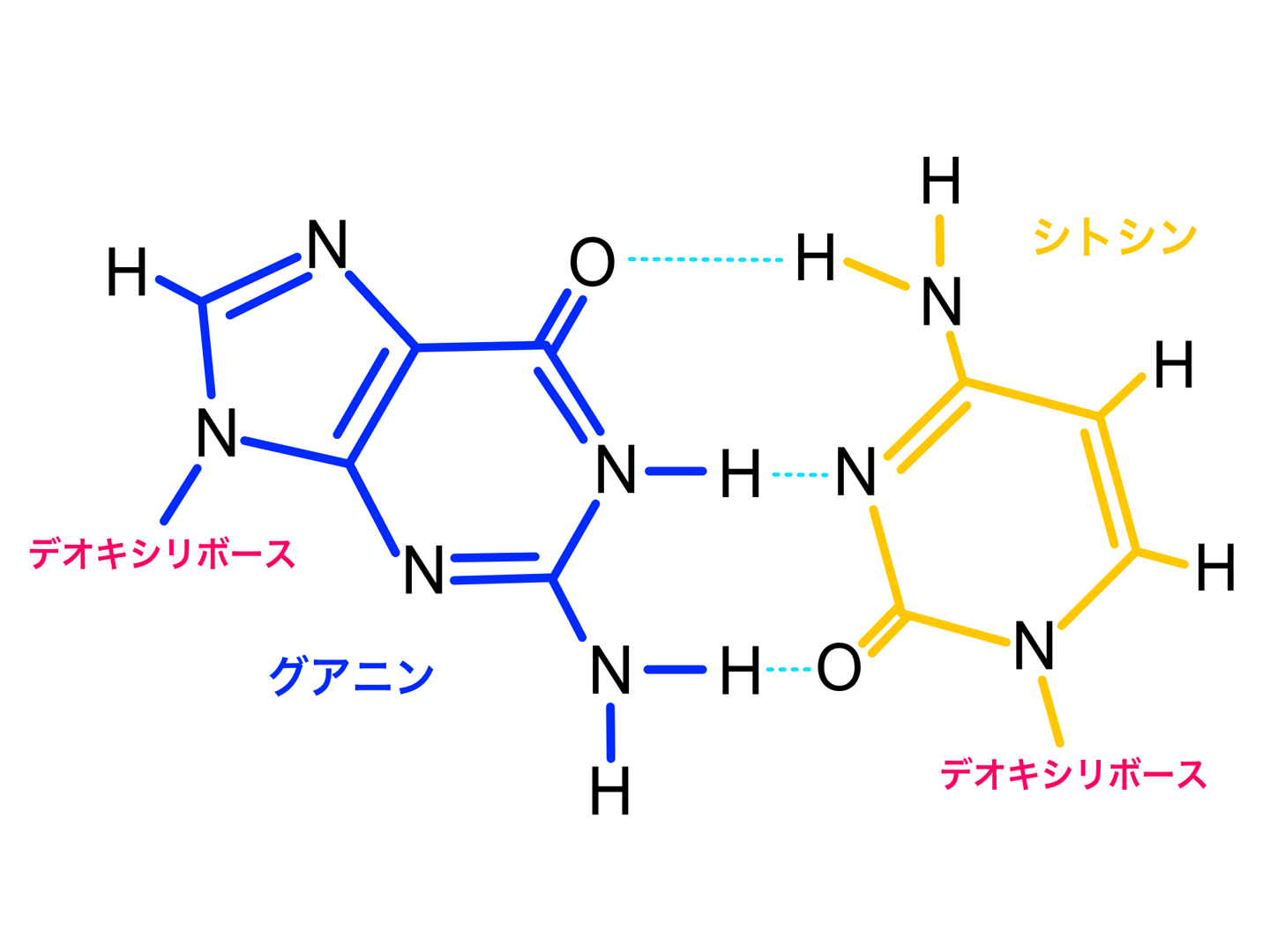
その他DNAの二重らせんなどにも水素結合は関わっています。二重らせん構造が崩れないように核酸塩基同士が水素結合をしています。この結合のルールとして以下のようになります。
- アデニン(A)とチミン(T)が水素結合2本で結合
- グアニン(G)とシトシン(C)が水素結合3本で結合
この水素結合は、水溶液中で加熱、又はアルカリを加えたりすることで切れて二重らせんがほどけて、一本鎖DNAとなります。このことを変性と言います。変性が進むと核酸塩基がむき出しになるため吸光度が増します。これを濃色効果と言います。
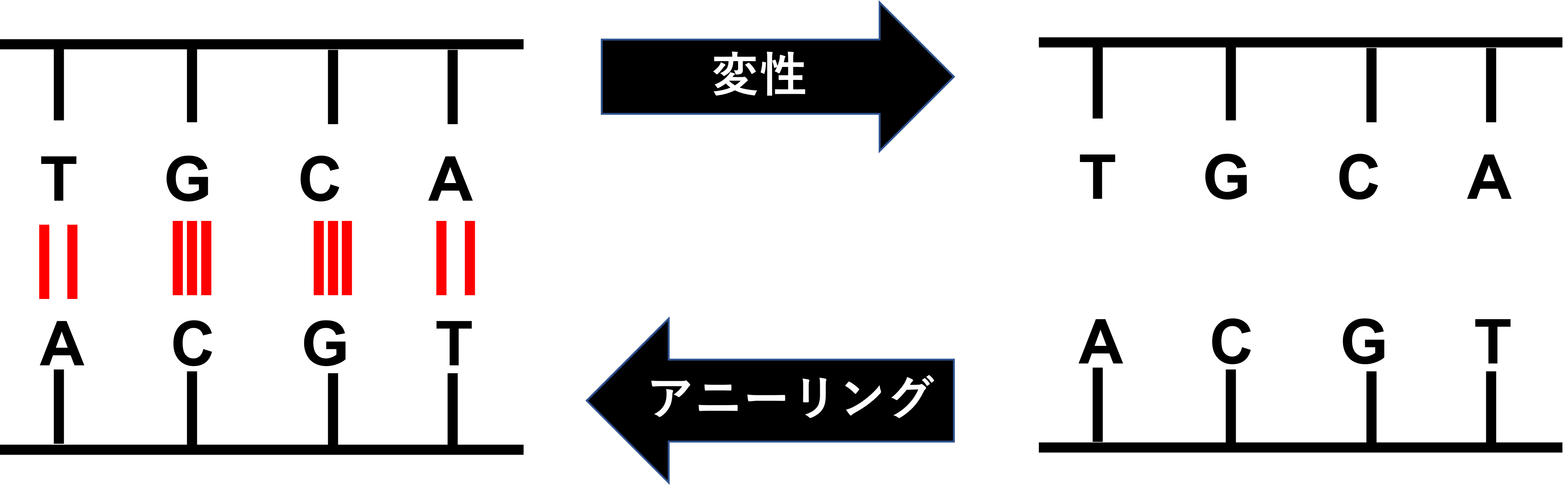
変性は可逆的なので、再び水素結合を形成することができます。この水素結合形成をアニーリングと呼びます。
Sponsored Link
Sponsored Link
水の水素結合
高校の内容になりますが、水素結合によって氷(固体)、水(液体)、水蒸気(気体)とそれぞれの状態で様々な性質をしまします。
まず氷は水素結合によって規則正しく配列しているため、隙間が大きく水よりも体積が大きくなります。しかし加熱によって水素結合が切れると隙間に滑り込むため、体積が減り密度が増えます。

このように、水素結合はファンデルワールス力よりも結合力が強く、密度や沸点に影響を与えます。その他にも溶解性にも影響を与え一般的に水素結合をつくるものどうしは溶けやすく、水素結合をつくるものと、作らないものでは溶けにくくなります。
次に疎水性相互作用を見ていきます。
疎水性相互作用
水溶液中に疎水分子が存在すると、疎水分子の無極性部分がファンデルワールス力によって会合して安定化します。このような作用を疎水性相互作用といいます。
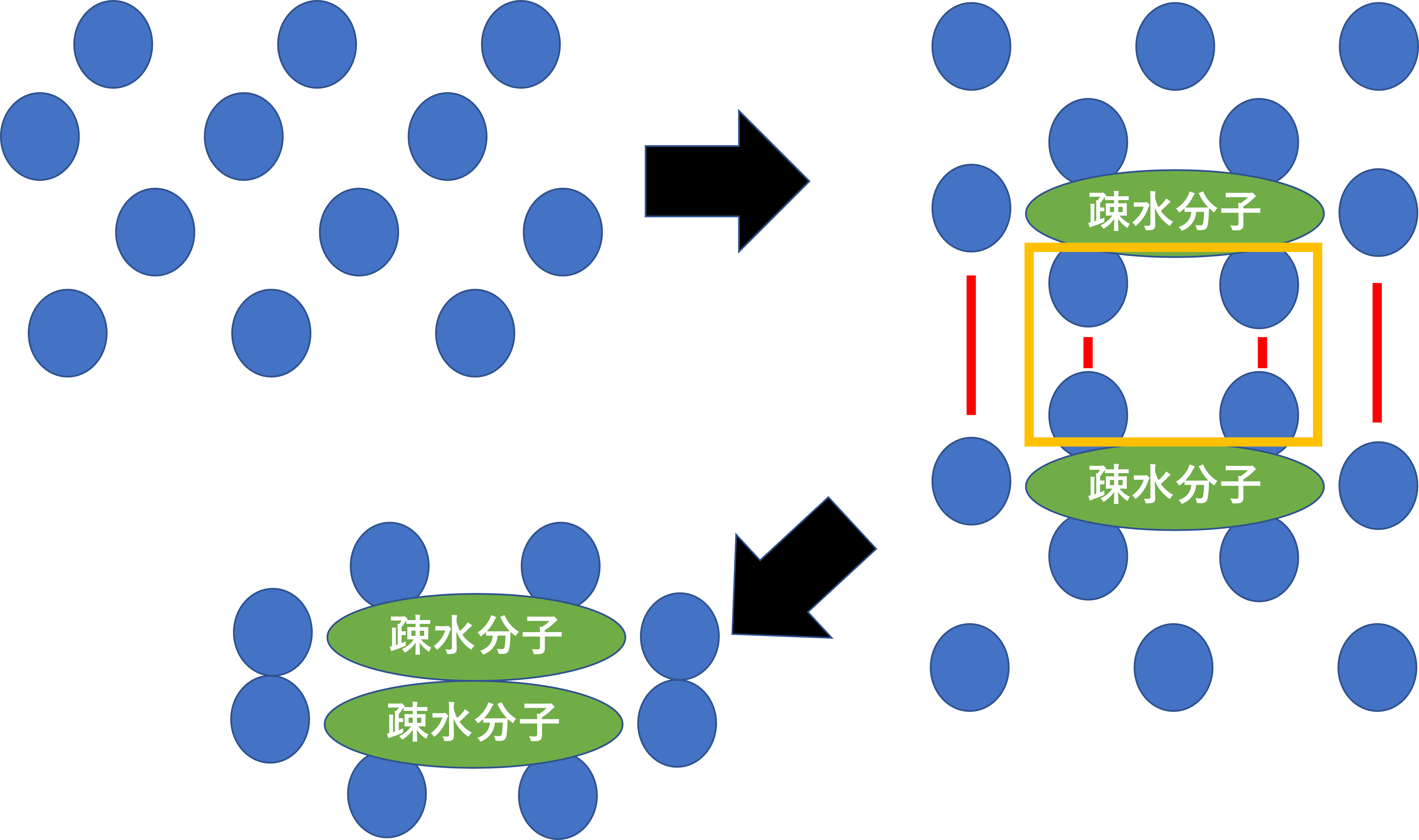
例えば水を例にしてみると、水どうしが近づくために水素結合をしようとします。そうすると、オレンジのところが邪魔なのでどかそうとします。これを水和水排除効果と言い、どかされた水は自由水として排出されます。そして疎水分子が会合します。
疎水性相互作用は、界面活性剤のミセル形成などに関わります。界面活性剤中の親水性部分が水と接触しようとする力が働いて、結果的に親水性部分に囲まれた内側で疎水性部分がファンデルワールス力によって安定化します。
まとめ
- 水素結合はDNAの二重らせんなどに関わっている。
- 疎水性相互作用はミセル形成などに関わっている。
