

Sponsored Link
RS配置、優先順位のつけ方
前回のZ配置やE配置、優先順位のつけ方ではZ配置やE配置を見ました。今回はRS表示について見ていきたいと思います。
今回も立体空間把握能力が問われます(笑)
RS表示
メタンCH4のように、炭素原子についている原子が水素だけならば、どの水素も変わりなく1つだけのメタンに落ち着きます。
しかし炭素についている原子が全て違う時には、1つに定まりません。例えばアラニンを見てみると、以下の2つが考えられます。
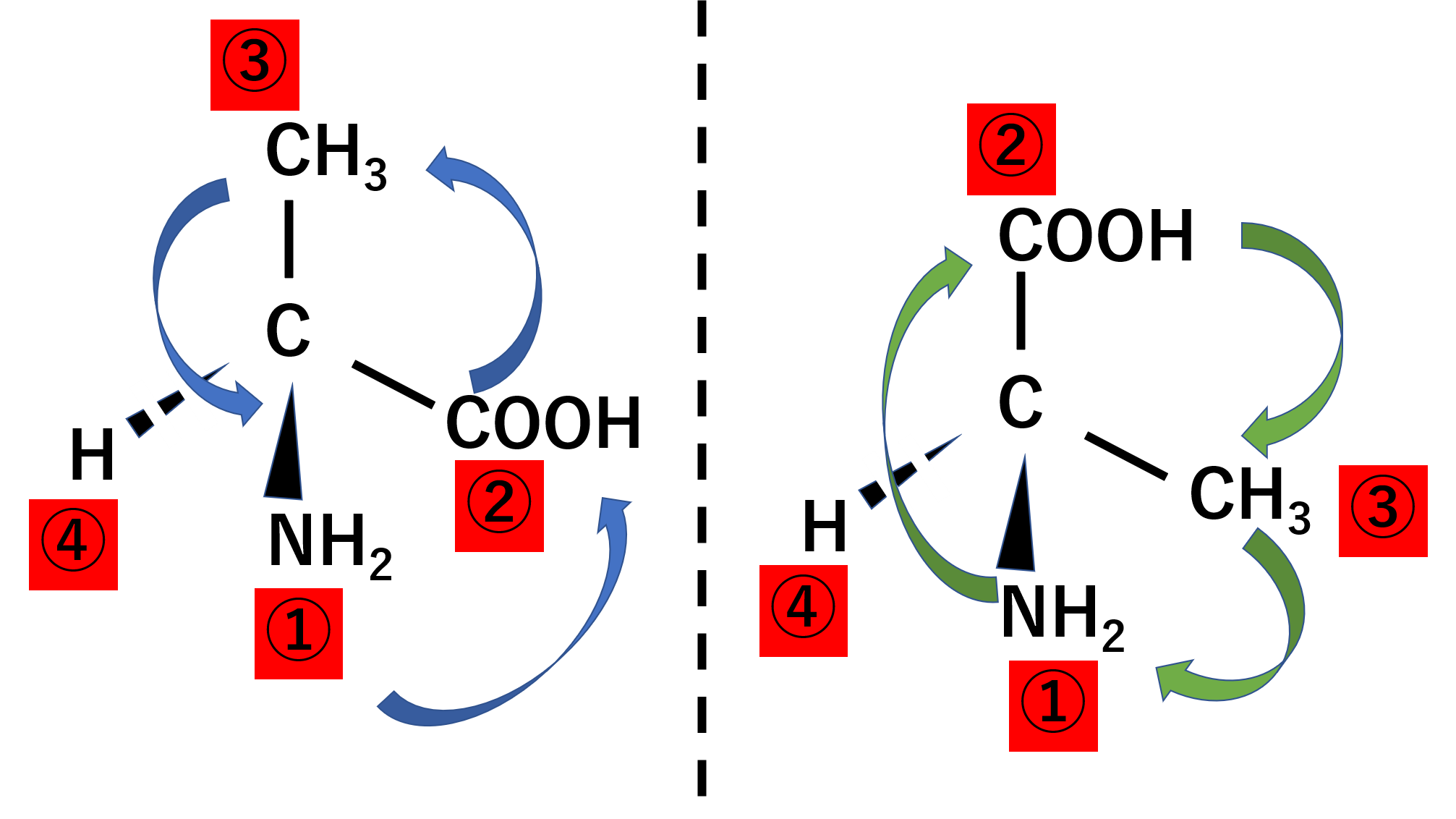
このような時に使われるのがRS表示です。前回のZ配置やE配置を決める時に使った優先順位のルールに則り、炭素原子についているその他の原子に優先順位をつけます。優先順位の④番目を奥に置いたときに、残りの①、②、③が時計回りならR配置となります。逆に①、②、③が反時計回りならS配置となります。
どっちがどっちか混乱してしまう人は、R配置は右回りなのでRをright(右)と強引に覚えましょう。消去法で反対はS配置と覚えられます。
これも習うより慣れよなので、早速例題を見ていきましょう。
Sponsored Link
Sponsored Link
例題1
次の化合物の不斉炭素はR配置かS配置か答えよ。

まず右側の炭素のまわりを優先順位をつけると反時計回りになるのでS配置となります。
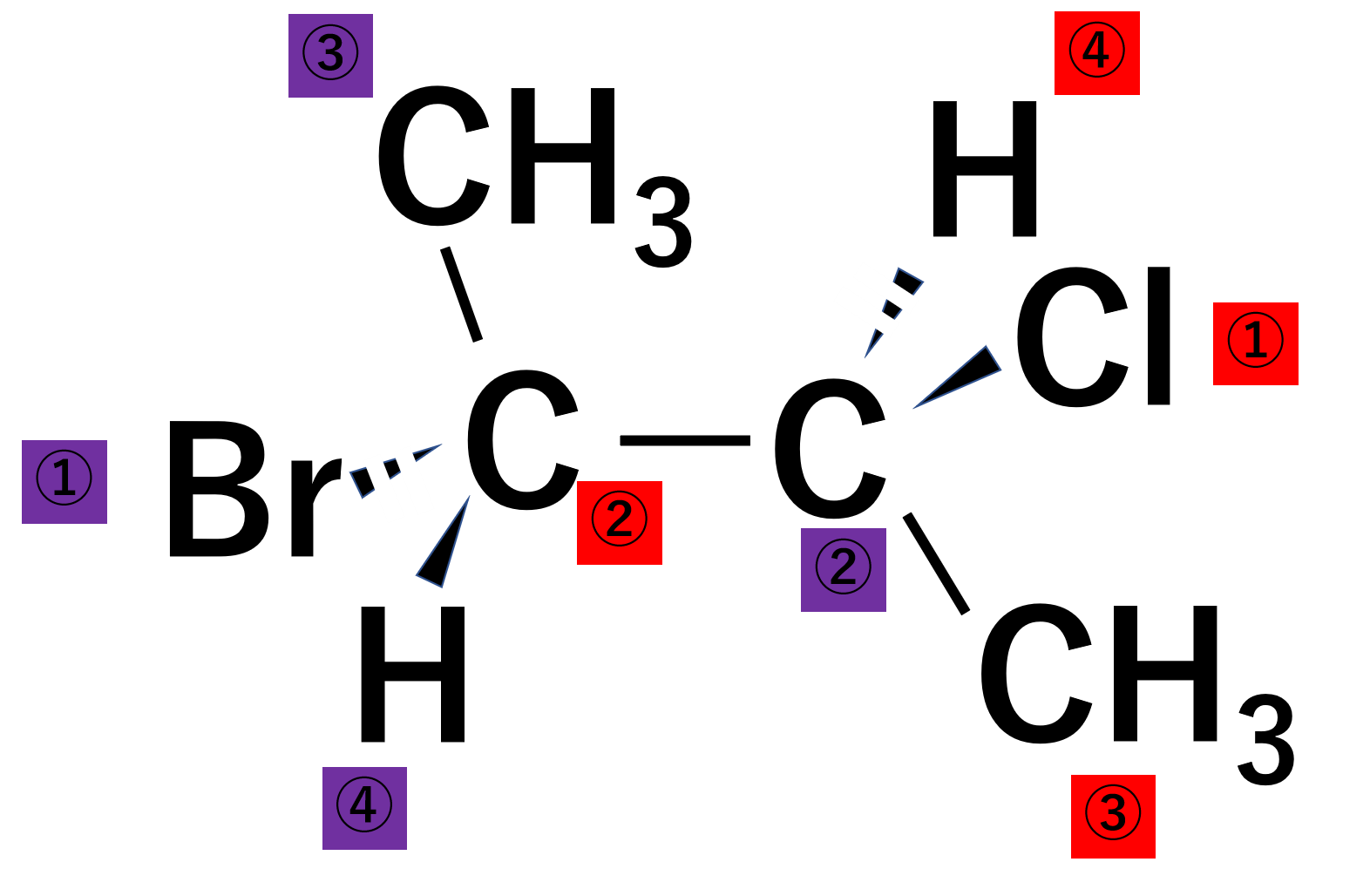
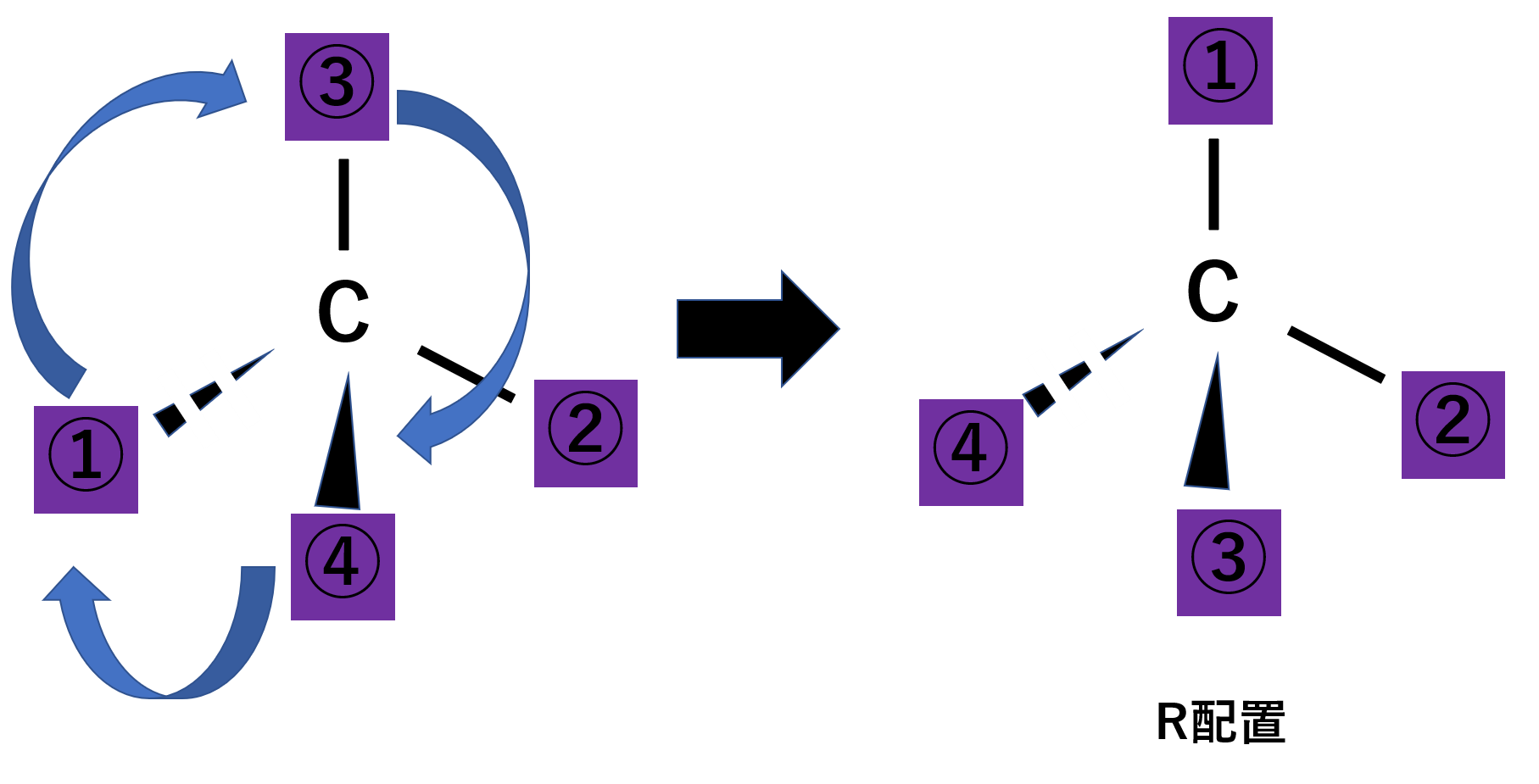
次に左側の炭素のまわりの優先順位をつけると反時計回りになりますが、注意するべきは④番目の水素が手前にあることです。RS表示は④番目を奥に置いたときに、残りの①、②、③で決めるというルールですので、反時計回りは逆の時計回りとなります。気になる方は実際に④番目を奥に回転させて試してみてください。よってR配置が答えとなります。
例題2
次の化合物の不斉炭素はR配置かS配置か答えよ。
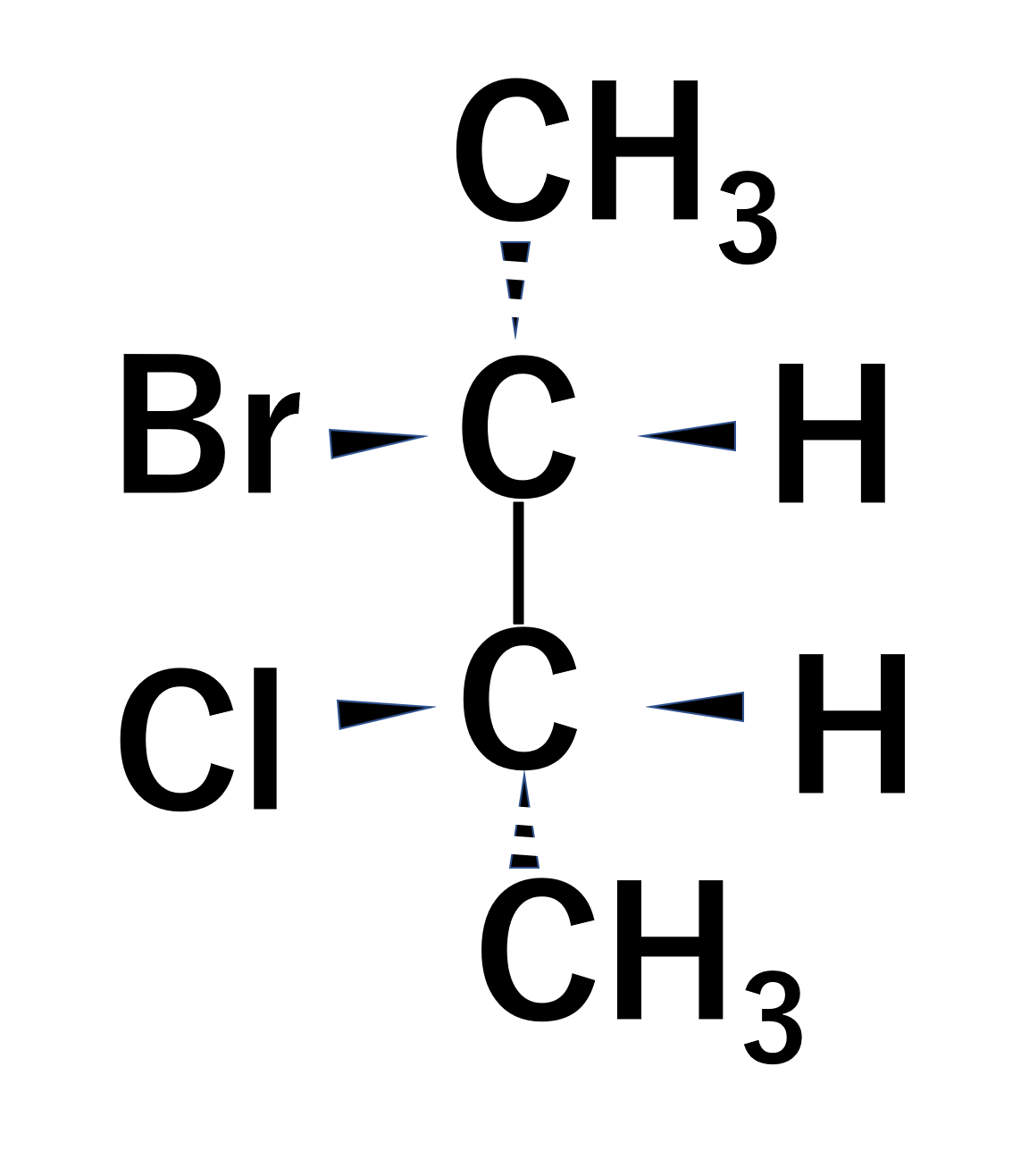
今度はFischer投影式のパターンです。
それぞれの優先順位をつけると以下のようになりますが、両方の炭素とも先ほどのように④番目の水素が手前に向いているため注意が必要です。
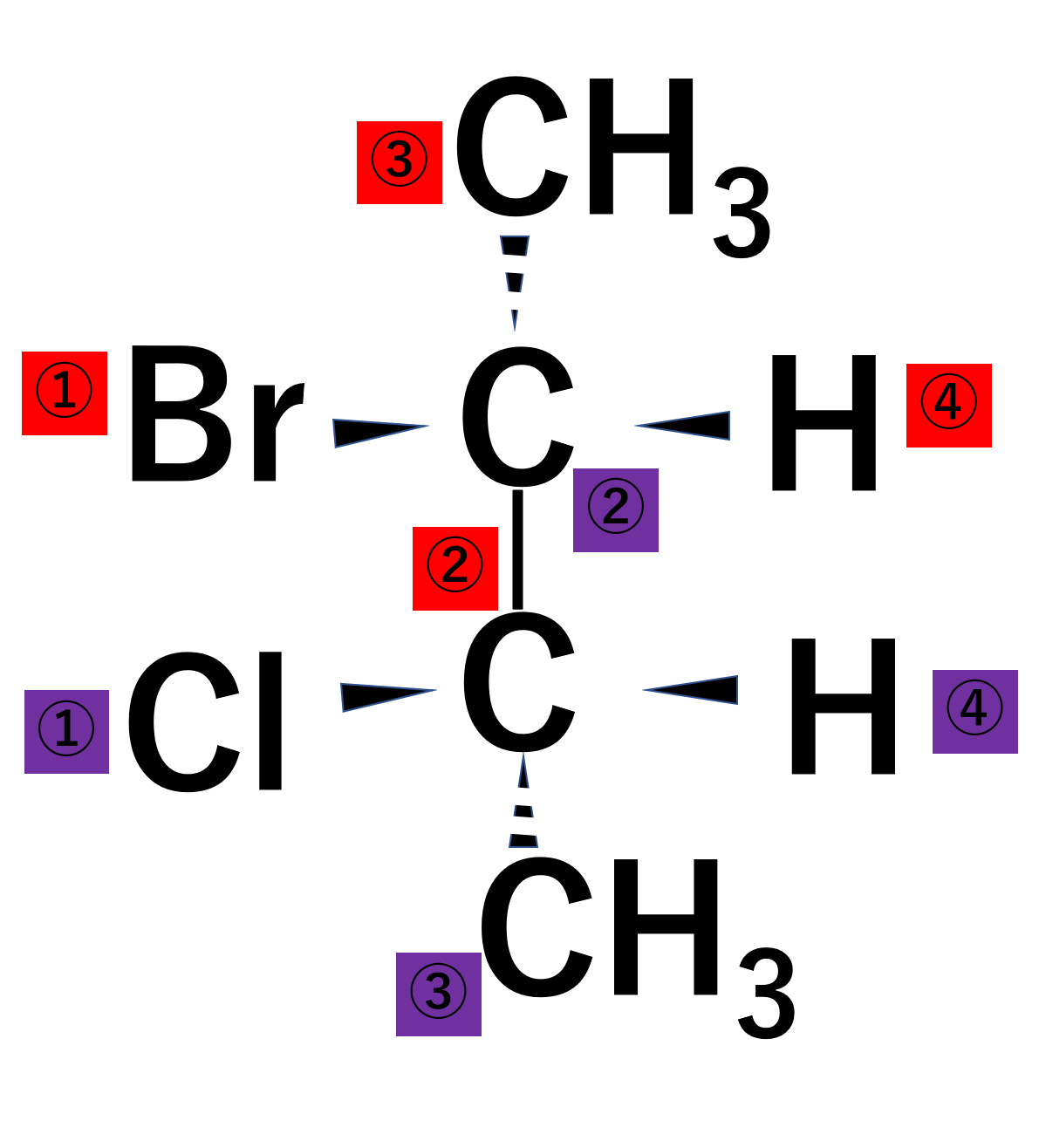
よって上の炭素がR配置、下の炭素がS配置となります。
例題3
次の化合物の不斉炭素はR配置かS配置か答えよ。

今度はNewman投影式のパターンです。
ここまでくると頭の中でできる方はいいですが、できない方はいったんFischer投影式に戻した方が間違えません。少し回転させて書き換えると以下のようになります。
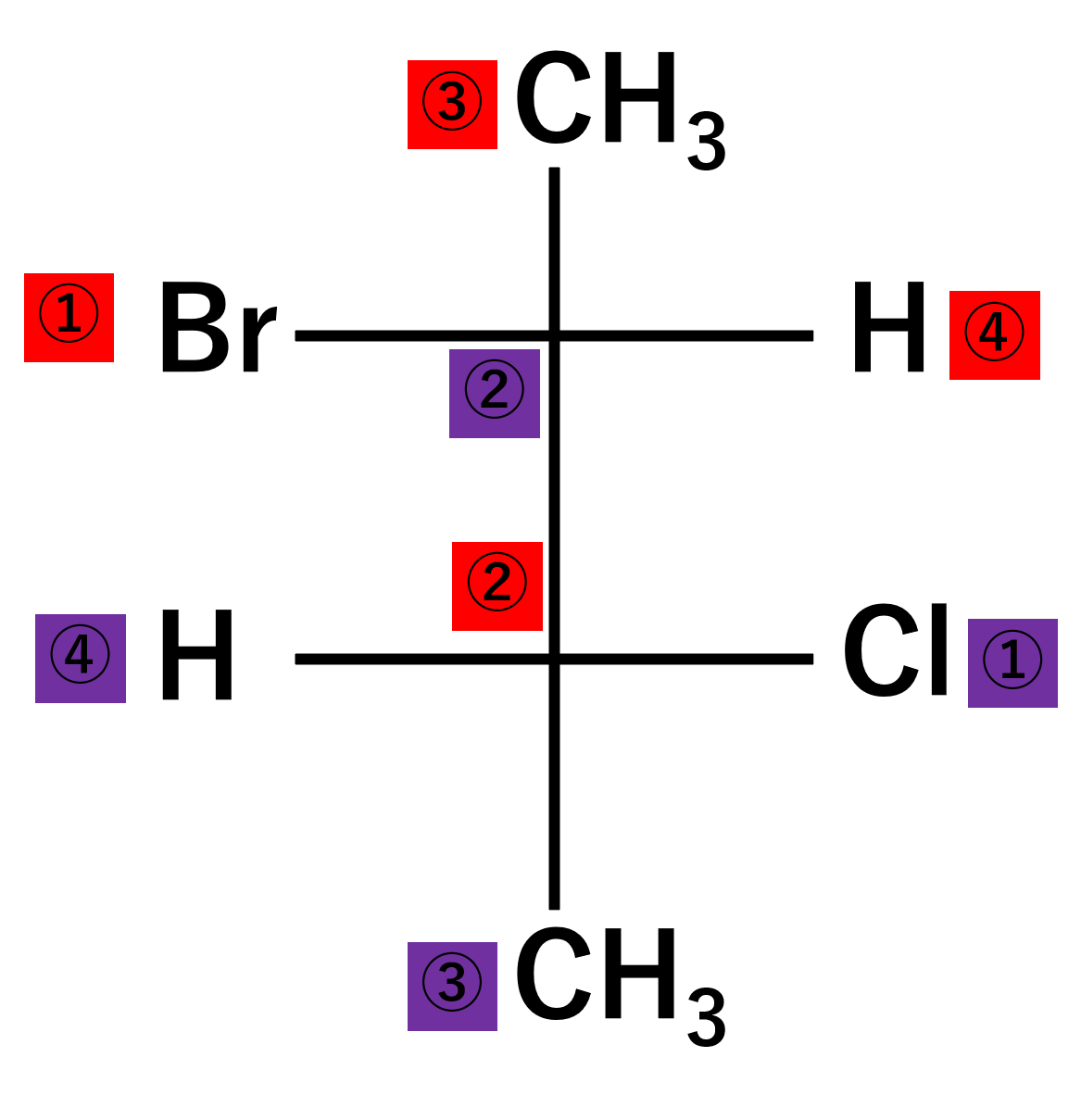
それぞれ優先順位をつけていくと、上の炭素がR配置、下の炭素がS配置となります。
まとめ
- 不斉炭素に優先順位をつけて、④番目を奥に置いたときに時計回りがR配置、反時計回りがS配置。
