

Sponsored Link
液体クロマトグラフィーと種類
前回のガスクロマトグラフィーと検出器ではガスクロマトグラフィーについて見ました。今回は液体クロマトグラフィーについて見ていきたいと思います。
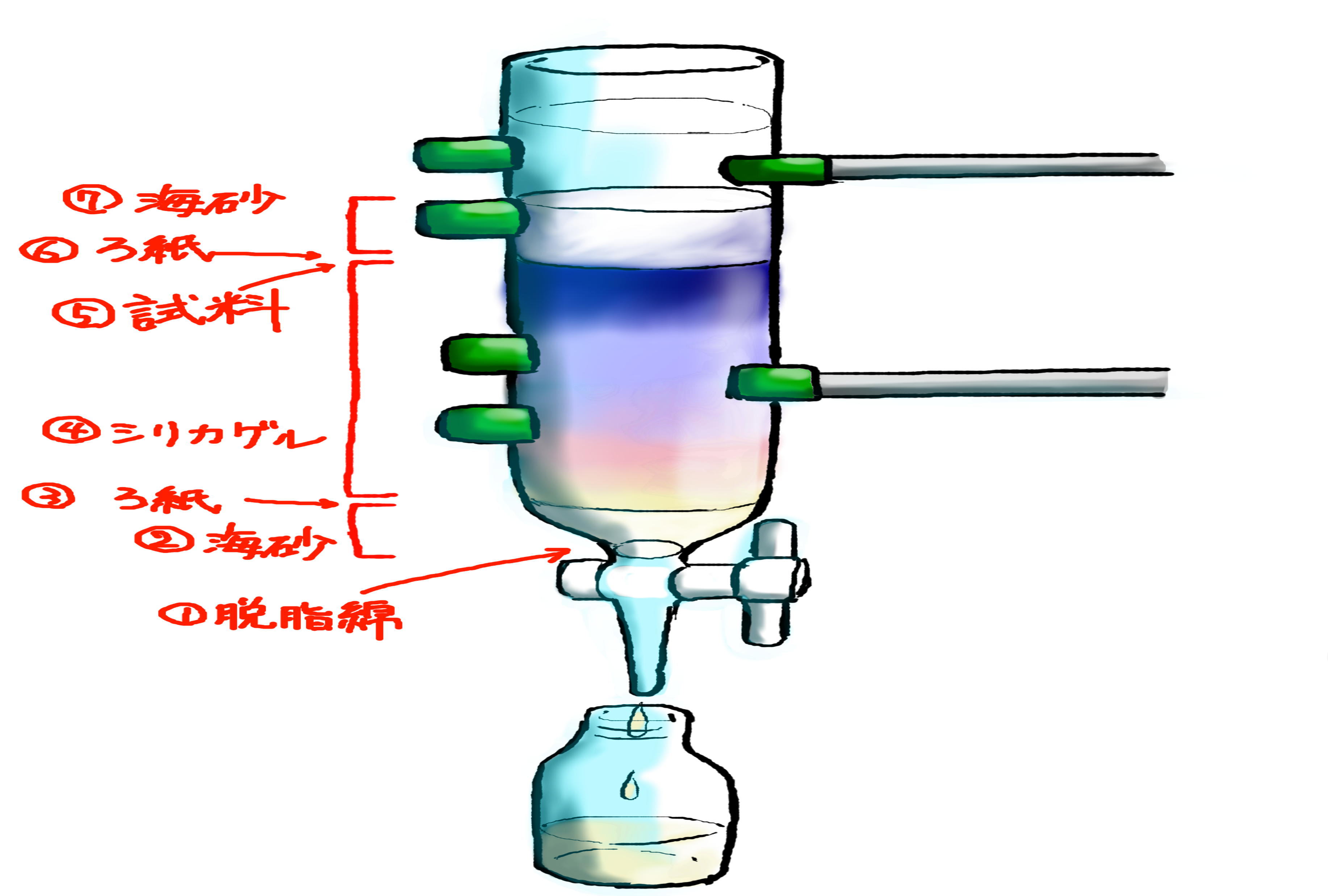
液体クロマトグラフィー
液体クロマトグラフィーの装置は、移動相送液用ポンプ、試料導入装置、カラム、検出器、記録装置などからなります。
液体クロマトグラフィーはカラムに試料混合物を注入して、移動相に液体を使って分離する方法です。液体クロマトグラフィーはガスクロマトグラフィーと比べて試料導入部やカラムを高温にする必要はないので、熱に不安定なものでも分析できます。液体クロマトグラフィーは固定相の違いにより以下のようなものがあります。
- 吸着クロマトグラフィー
- 分配クロマトグラフィー
- イオン交換クロマトグラフィー
- ゲルクロマトグラフィー
Sponsored Link
Sponsored Link
吸着クロマトグラフィー
吸着クロマトグラフィーはヘキサンやクロロホルムなどの極性の低い溶媒を移動相に、シリカゲルやアルミナなど極性が高く吸着能が高い固定相に用いたものです。中でもシリカゲルはよく使われ、シリカゲルの表面に存在するシラノール基が水素結合をするため、極性の高い化合物ほど固定相に保持されます。

分配クロマトグラフィー
分配クロマトグラフィーは、固定相に極性の高い溶媒、移動相に極性の低い溶媒を組み合わせの順相分配クロマトグラフィー、固定相に極性の低い溶媒、移動相に極性の高い溶媒を組み合わせの逆相分配クロマトグラフィーにわけられます。

中でも逆相分配クロマトグラフィーには、固定相にオクタデシルシリル化シリカゲルがよく使われ、極性の低い化合物ほどよく保持されます。オクタデシルシリル化シリカゲルとは、シリカゲルにC18の直鎖飽和炭化水素を導入したもので耐圧性に優れます。
イオン交換クロマトグラフィー
イオン交換クロマトグラフィーは、固定相にイオン交換性を持つものを用いるクロマトグラフィーでアミノ酸の分離などに使われます。イオン交換クロマトグラフィーは移動相のpHや塩濃度に影響を受けます。
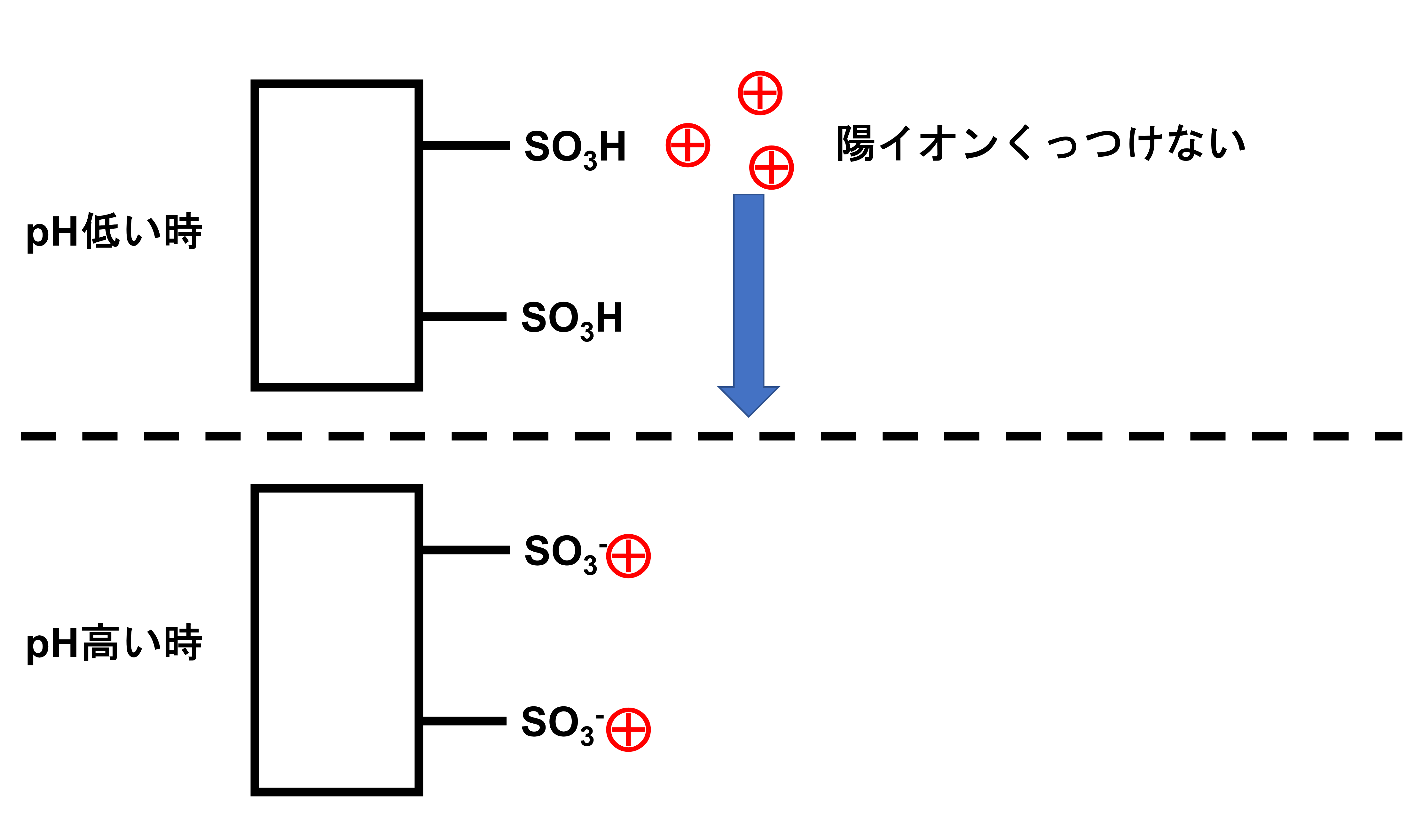
例えば固定相によく使われるポリスチレンスルホン酸型(陽イオン交換樹脂)は、移動相のpHが低い状態では、-SO3Hとなっていて陽イオンはくっつくことができません。逆にpHの高い状態では-SO3-となり陽イオンはくっつくことができます。
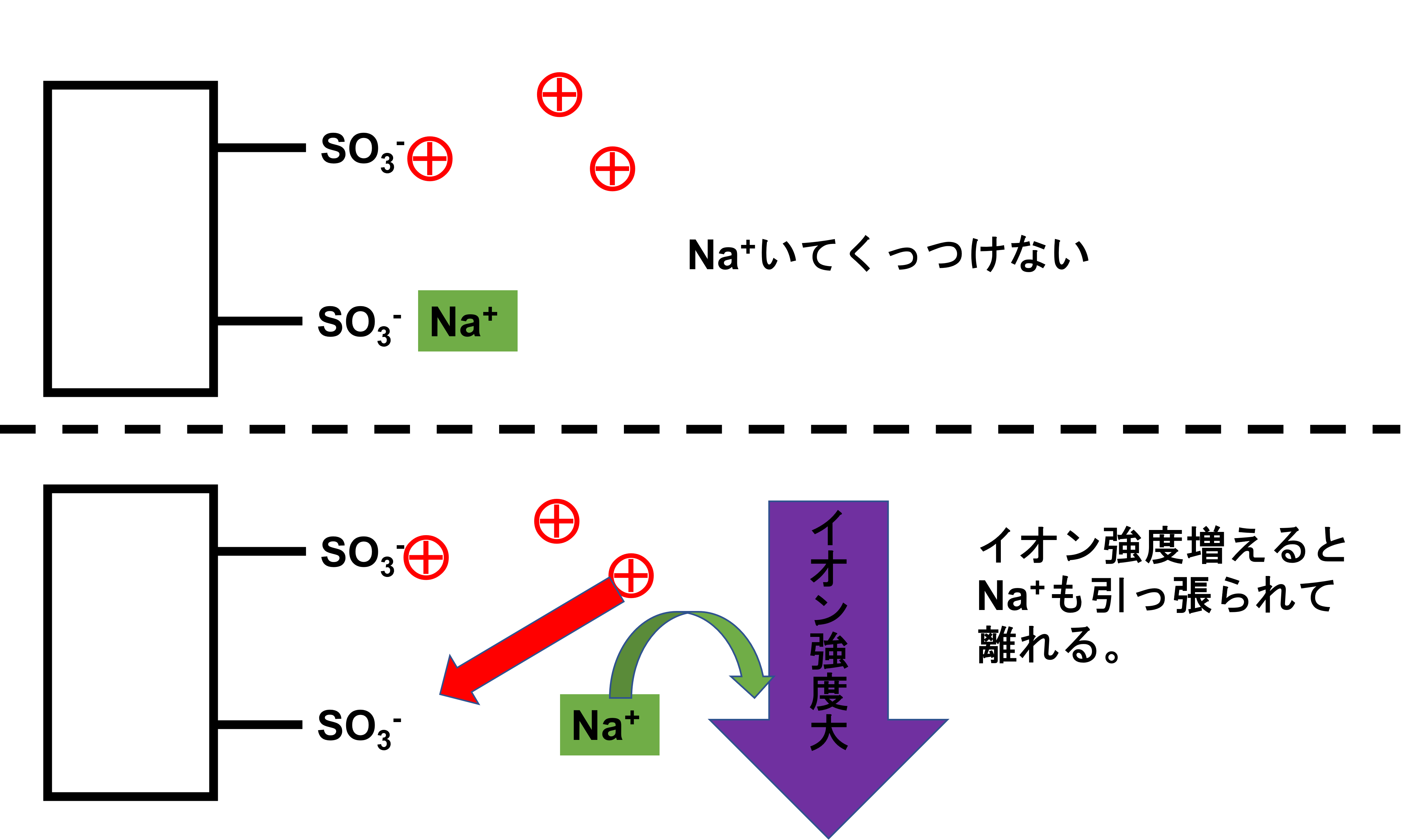
またポリスチレンスルホン酸型(陽イオン交換樹脂)における塩濃度を見てみると、例えば図の状態ではNaがいて陽イオンがくっつくことができません。そこにイオン強度が大きいものを移動相に流すと、Na+が移動相の陰イオンにくっついていくので、-SO3-のところがあき陽イオンがくっつくことができます。
一方でアミノ酸は両性化合物であるため、pHの低い状態では陽イオンとなり、pHの高い状態では陰イオンとなります。この性質から、pHの低い状態ではポリスチレンスルホン酸型(陽イオン交換樹脂)にくっついています。そしてだんだんとpHを上げていくことで陰イオンに近づいてくるためポリスチレンスルホン酸型(陽イオン交換樹脂)から離れていきます。よって等電点の低いアミノ酸から順番に溶出していくので分離できるわけです。
このようにして分離したアミノ酸は、ラベル化と呼ばれる方法で検出しやすくして検出します。どの時点で検出するかで以下の2つにわけられます。
- プレラベル法;前処理段階で試料をラベル化して、カラムに注入。ラベル化した資料をカラム出口で検出。
- ポストラベル法;試料をカラムに注入し、カラム出口で試料にラベル化剤を加えて検出。
プレラベル化法ではカラムにラベルが落ちて汚れやすいため、あまり使われません。そのためポストラベル法が一般的で、ラベル化剤にはニンヒドリンやオルトフタルアルデヒドなどが使われます。ニンヒドリンは紫外線検出、オルトフタルアルデヒドは蛍光検出で、覚えるためのゴロです。
- ポストに死骸オッケー

- ポスト;ポストラベル法
- に;ニンヒドリン
- 死骸;紫外
- オ;オルトフタルアルデヒド
- ケー;蛍光
解説するまでもないですが、良い子はポストに死骸を入れないようにしてください(笑)
ゲルクロマトグラフィー
ゲルクロマトグラフィーは、三次元網目構造をもつ多孔性の非イオン性ゲルを固定相に用いたクロマトグラフィーです。分子量の大きいものほどゲルの網目に引っかからないので先に溶出されます。

まとめ
- 液体クロマトグラフィーは固定相により吸着クロマトグラフィー、分配クロマトグラフィー、イオン交換クロマトグラフィー、ゲルクロマトグラフィーなどにわけられる。
