

Sponsored Link
2成分の気液平衡の状態図
前回の状態図と自由度では状態図について見ました。前回までのは1成分だけでしたが、今回は2成分の状態図について見ていきたいと思います。
2成分の状態図
ここでは成分Aと成分Bの混合物に対して、気液平衡について見ます。
まず縦軸が何であるかどうかをしっかり確認します。一般的な問題では温度が縦軸ですが、圧力が縦軸の場合は後で説明する上の曲線が液相線、下の曲線が気相線となるからです。
ここでは、縦軸が温度であるとして話を勧めます。

- 上の曲線;気相線
- 下の曲線;液相線
- Ta;Aの沸点
- Tb;Bの沸点
さて縦軸よりAの沸点よりBの沸点が高いことがわかります。そして今、「ア」の時点では組成がXの溶液となっています。
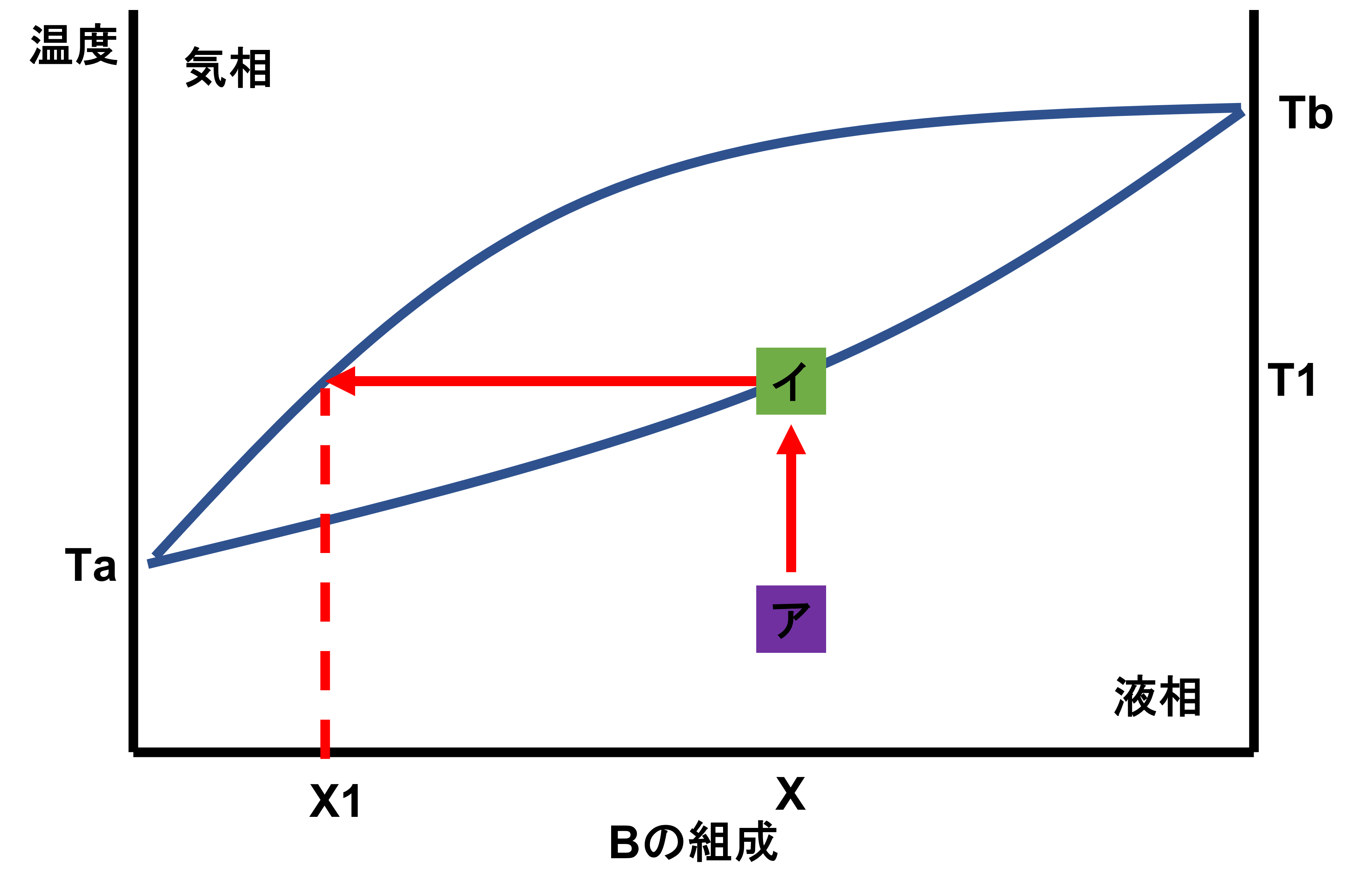
これを温度T1まで上げていきます。そうすると、「イ」で液相線にぶつかります。液相線より上の領域では気相と液相が混ざっている状態となり、気体が発生することになります。この時Bの組成がX1の気体が発生します。
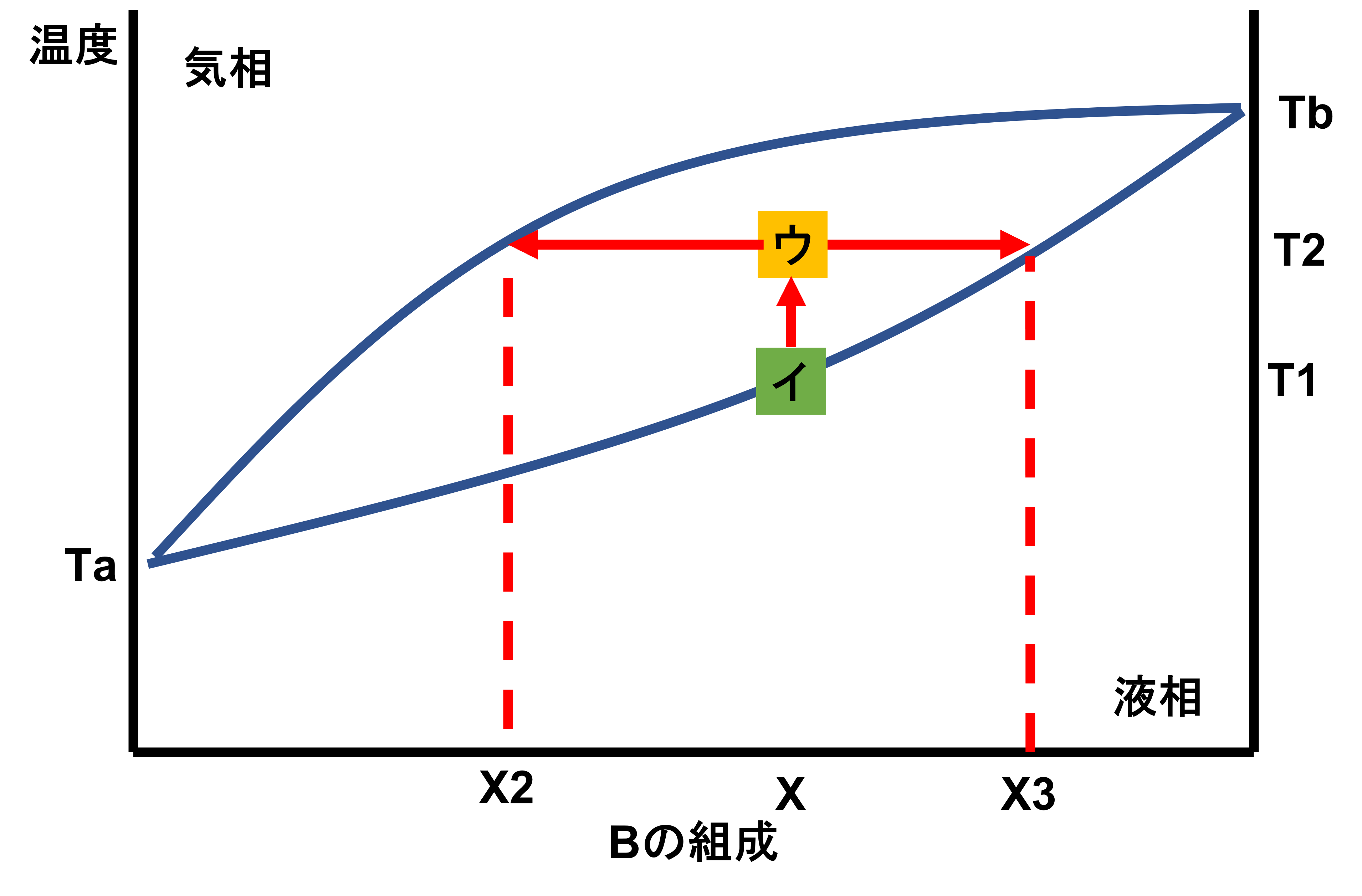
次に温度T2まで上げていき、「ウ」のところになった時は、気相中のBの組成がX2、液相中のBの組成がX3が共存した状態となります。この時の気相と液相の存在比は、(X3−X):(X−X2)となります。
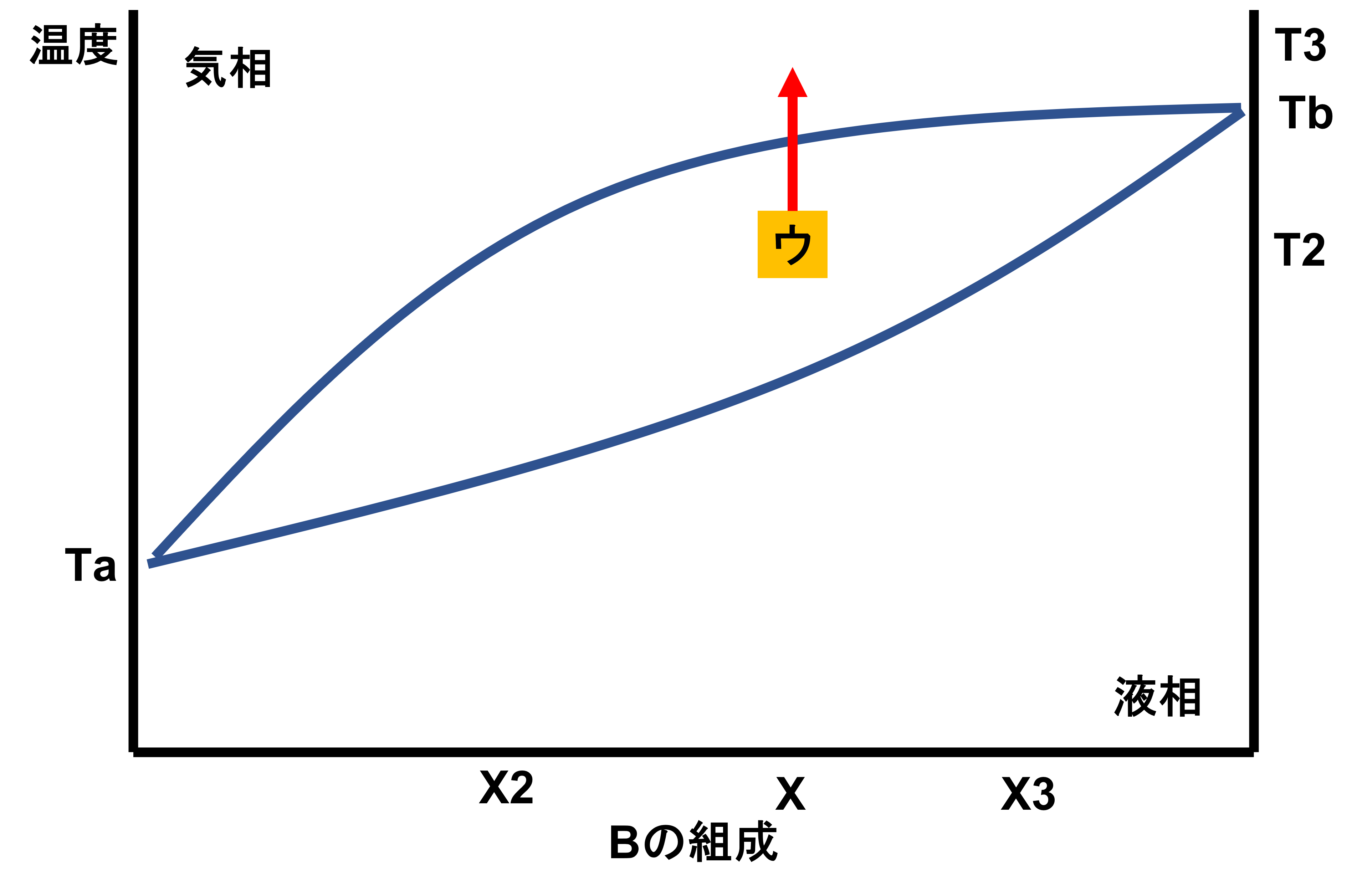
このまま温度をT3まで上げていくと、Bの組成がXの気体となることがわかります。
では、「ウ」の時点で得られた気相中の組成がX2のものを冷却したらどうなるでしょうか?
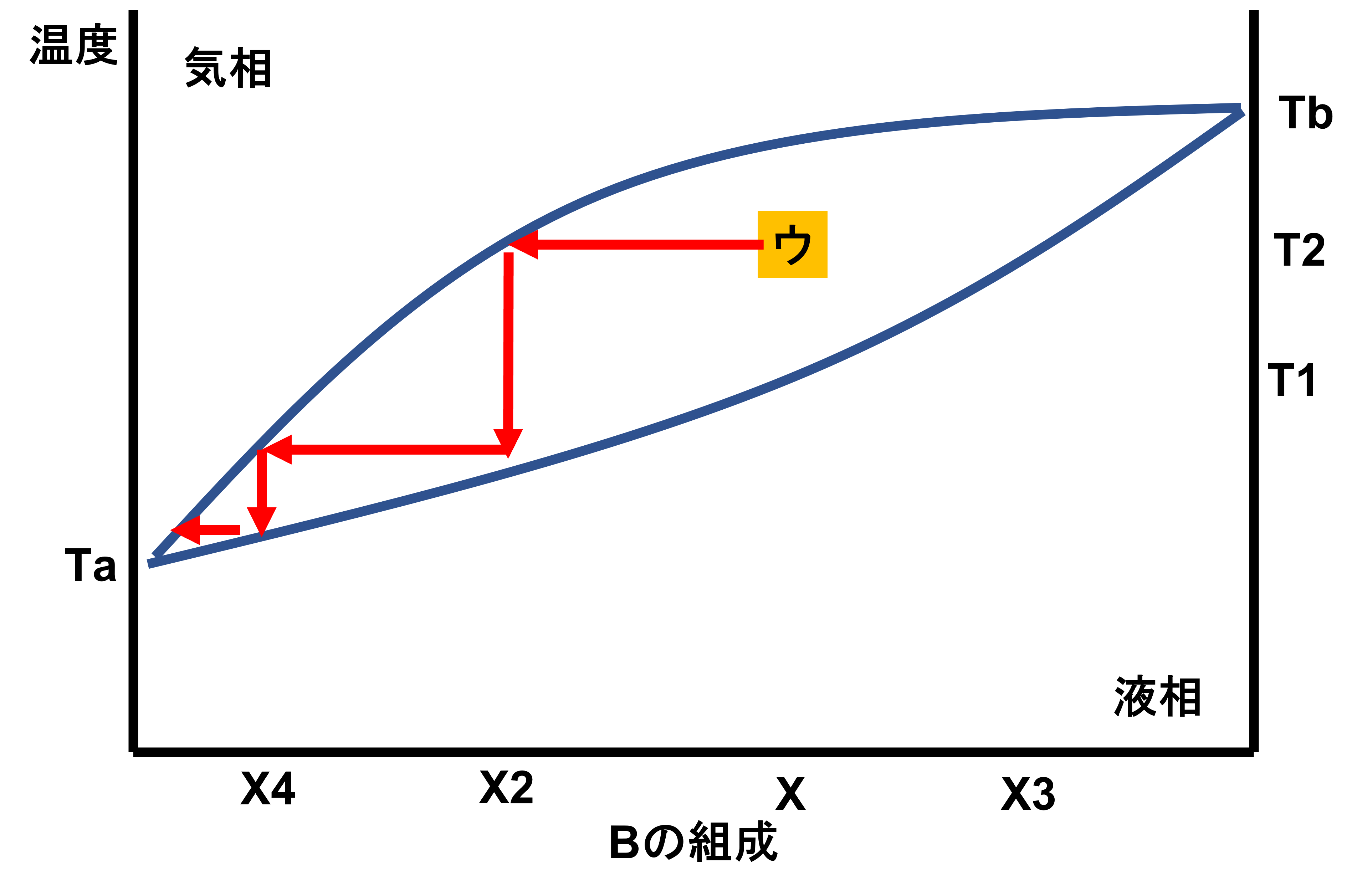
グラフとしては少し下に下がることになり、新たに気相中のBの組成がX4ののものが得られます。これを繰り返し続けることによって、蒸気からは純粋なAを抽出できることになります。
では基本をみたところで国試風の例題を見ていきます。
Sponsored Link
Sponsored Link
例題1
これはある成分Aと成分Bの混合物の液相気相の状態図である。P点にある混合物を温度上昇させたとき以下の正誤に答えよ。
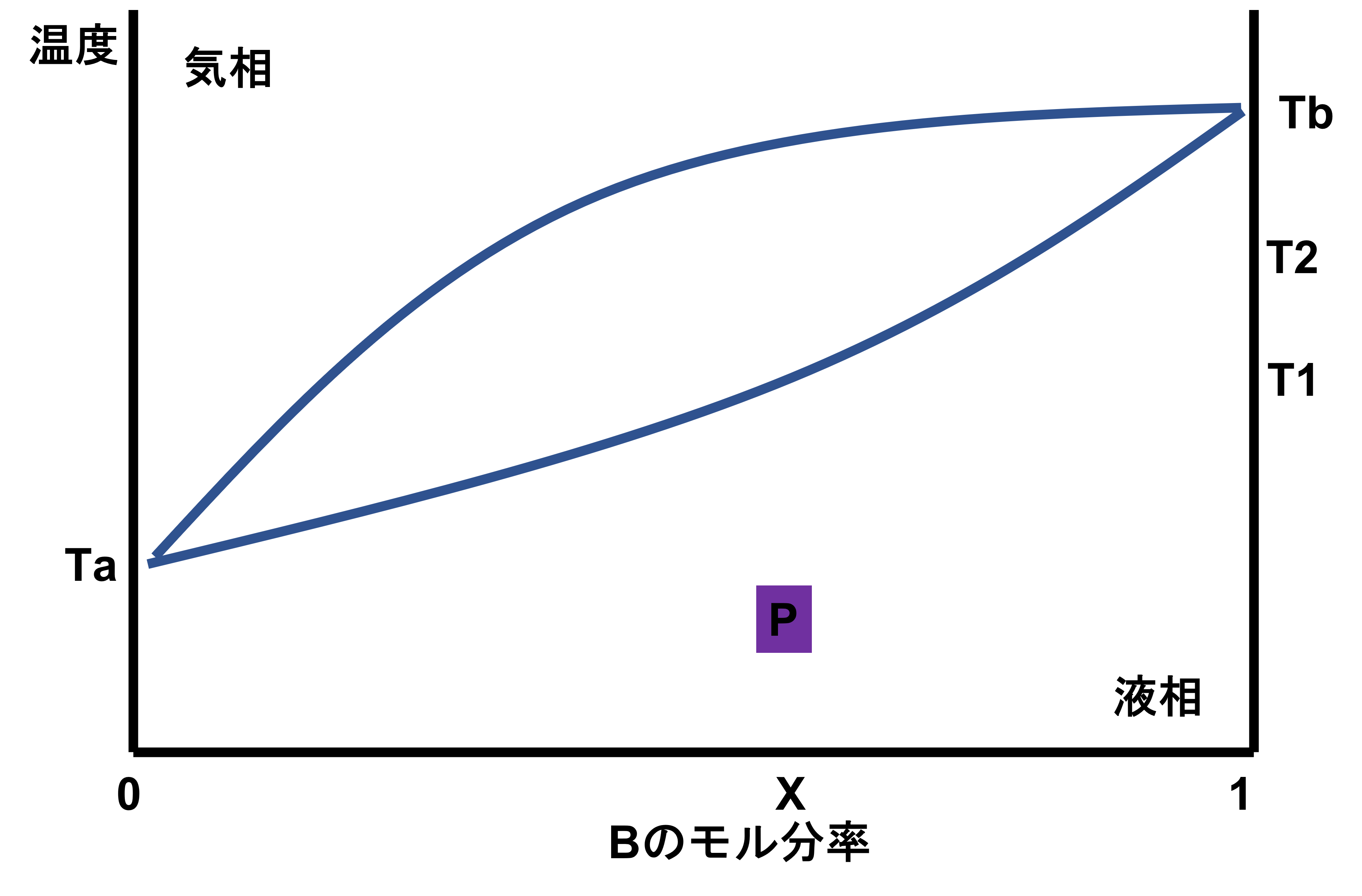
- 温度T1では気相が現れる
- 温度T2では液相中の成分Bのモル分率はXより大きい
- 温度T2では気相中の成分Bのモル分率はXより大きい
- 温度T1で蒸気を集めて冷却したものを再蒸留し、これを繰り返すとほぼ成分Bの蒸気が得られる
温度T1では気相が現れる
〇。T1の時点で、Bの組成がX1の気相が現れます。

温度T2では液相中の成分Bのモル分率はXより大きい
〇。T2の時点で、液相中のBの組成がX2となり、Xより大きいです。
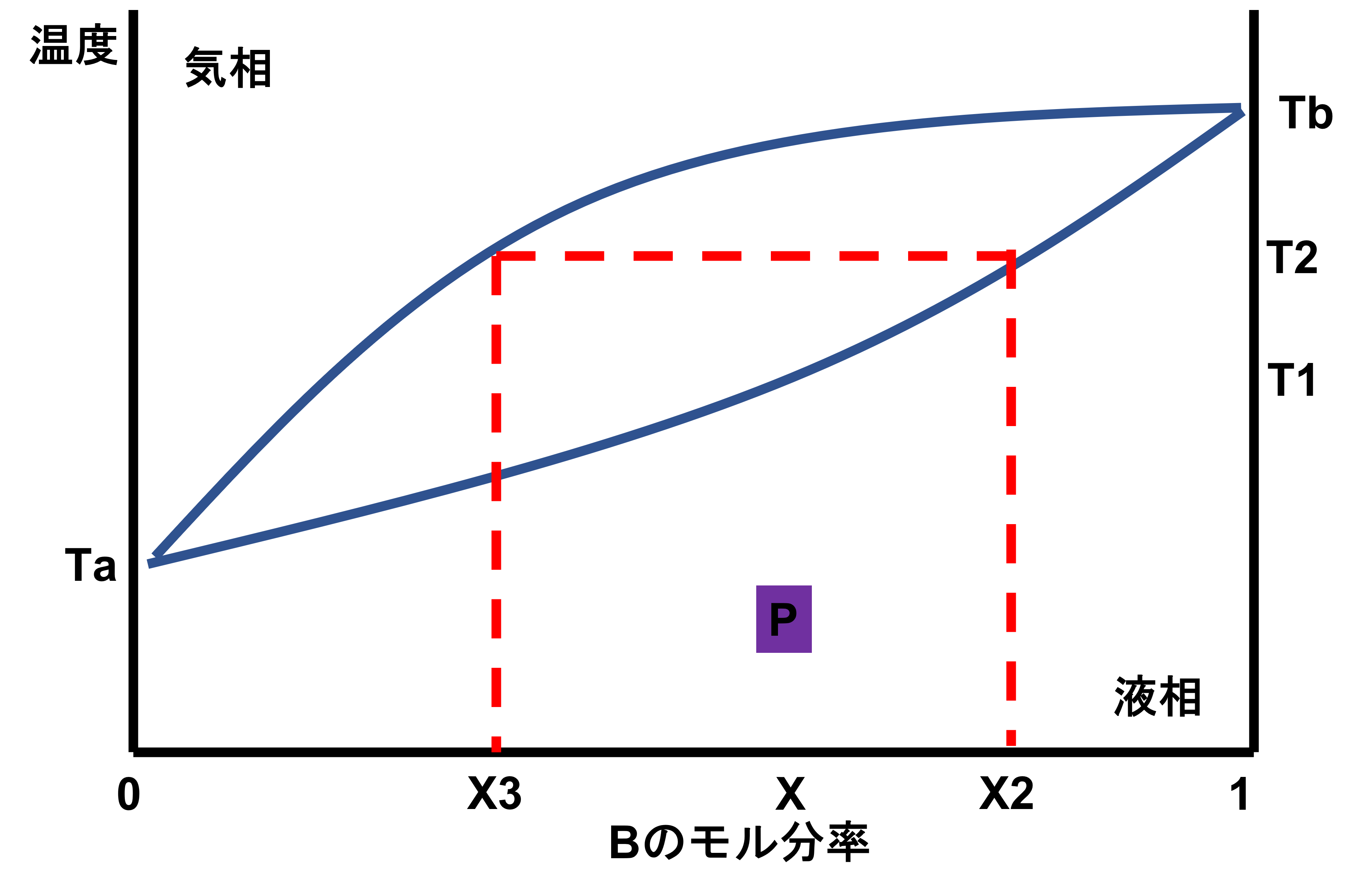
温度T2では気相中の成分Bのモル分率はXより大きい
×。T2の時点で、気相中のBの組成がX3となり、Xより小さいです。
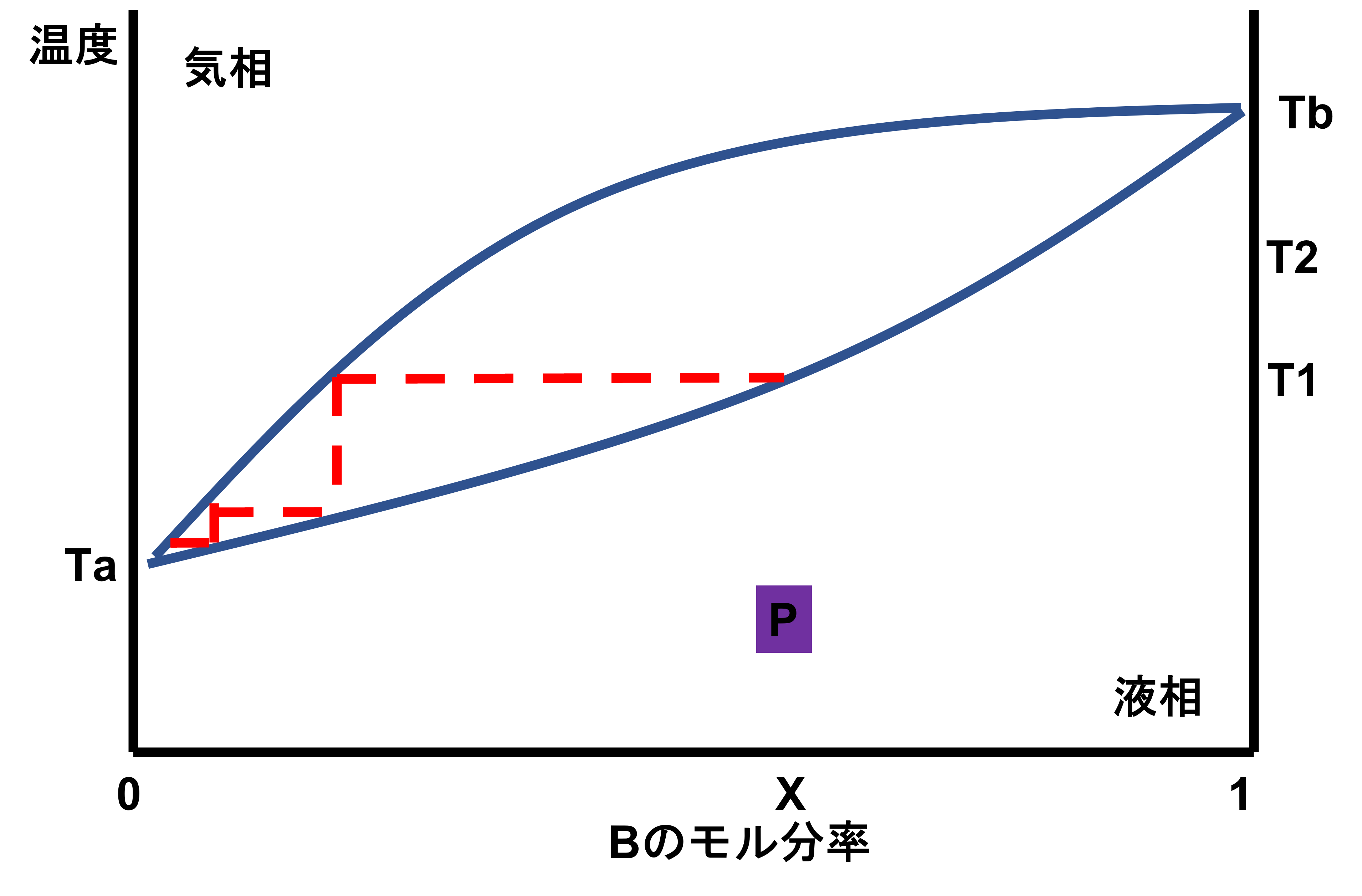
温度T1で蒸気を集めて冷却したものを再蒸留し、これを繰り返すとほぼ成分Bの蒸気が得られる
×。再蒸留を繰り返していくと、徐々にBの組成が少なくなっていき、純水なAの蒸気が得られます。
まとめ
- 2成分の気液平衡の状態図では、グラフをしっかりみて情報をまとめることが重要
