
実習生、新人薬剤師のための参考書

運動エネルギーと位置エネルギーの総和を内部エネルギーと言い、孤立系の内部エネルギーが一定であることを熱力学第一法則と言います。定容熱容量は定圧熱容量より小さくなります。
Sponsored Link
熱力学2、熱力学第一法則と熱容量
前回の熱力学1、系と状態関数のまとめでは、系などについて見ました。今回は熱力学第一法則について見ていきたいと思います。熱力学第一法則の前に内部エネルギーについて確認します。
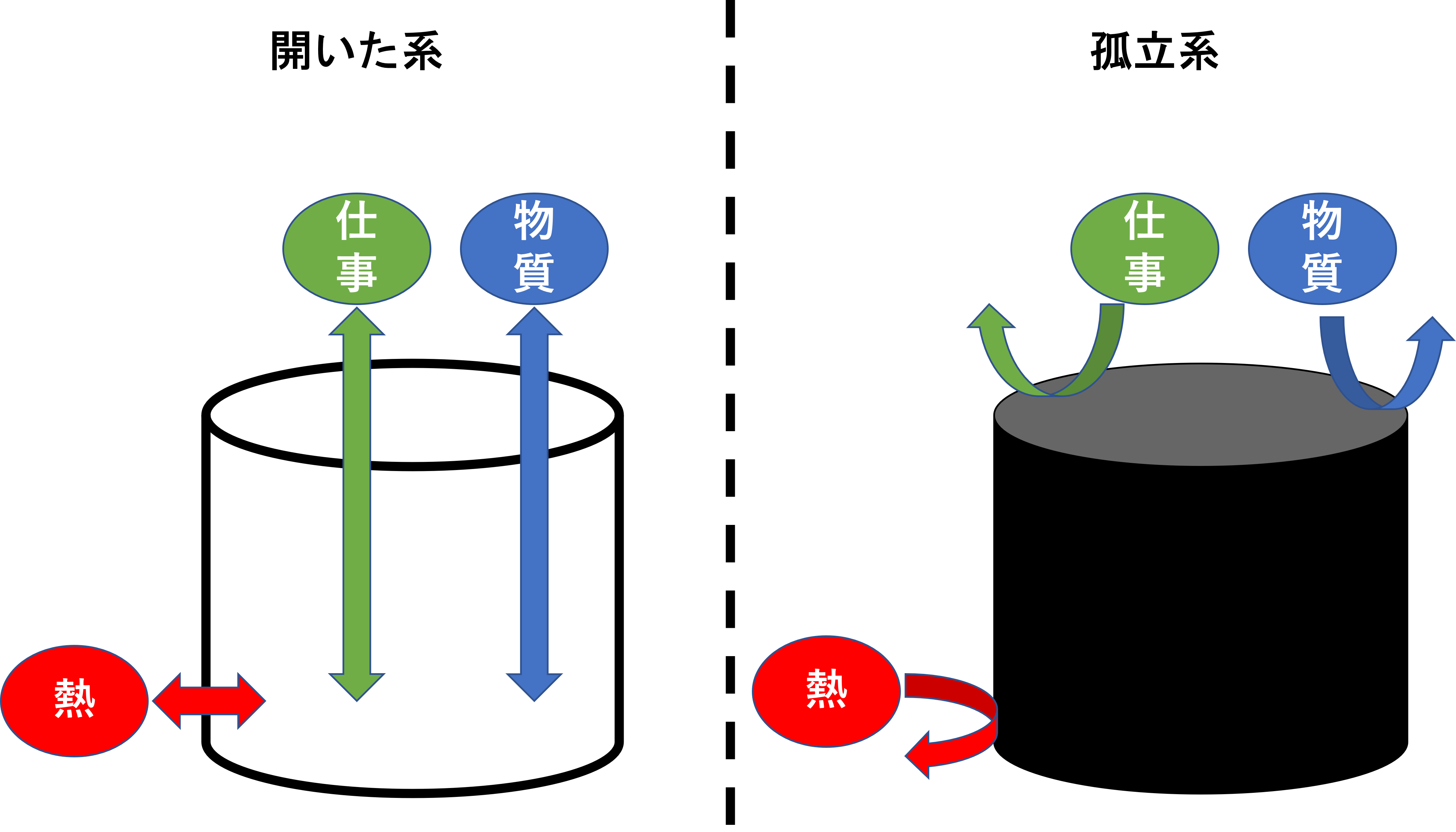
内部エネルギーU
物質系をつくる全ての原子や分子の持つ運動エネルギーと位置エネルギーの総和を内部エネルギーと言います。運動エネルギーや位置エネルギーには以下のようなものがあります。
- 運動エネルギー;並進エネルギー、回転エネルギー、振動エネルギー
- 位置エネルギー;電子エネルギー
運動エネルギーと位置エネルギーの総和である内部エネルギーですが、熱力学では仕事と熱の変化量(ΔU)について考えます。熱(q)と仕事(w)の変化には以下の4つのパターンが考えられます。
- 外から仕事が加えられる。外から熱が加えられる;ΔU=(+q)+(+w)
- 外へ仕事が放出される。外から熱が加えられる;ΔU=(+q)+(−w)
- 外から仕事が加えられる。外へ熱が放出される;ΔU=(−q)+(+w)
- 外へ仕事が放出される。外へ熱が放出される;ΔU=(−q)+(−w)
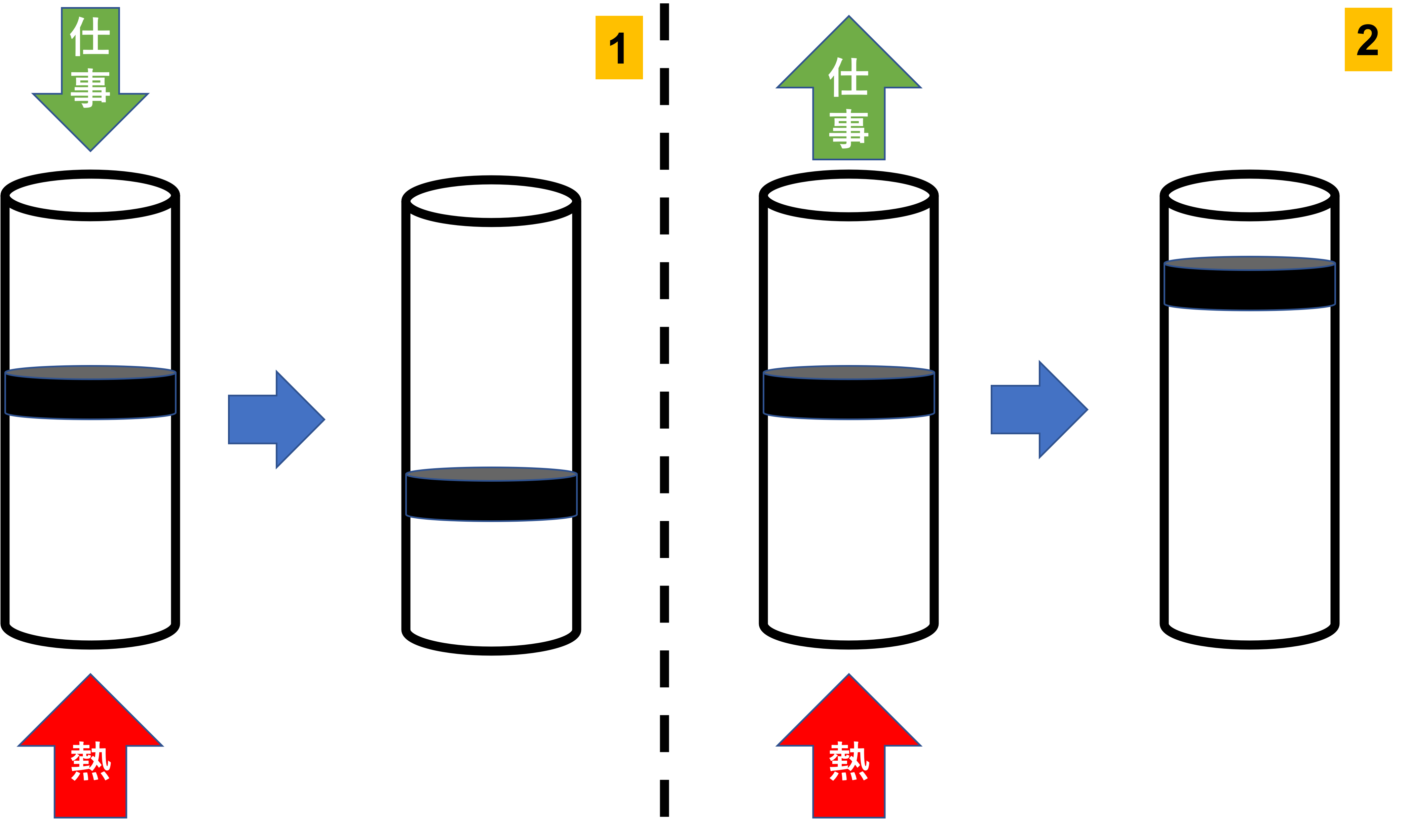

熱力学第一法則
熱力学第一法則は、孤立系においてエネルギーは相互に変換して形を変えることはあっても、新たに発生したり消失したりすることはなく、その総量はつねに一定という法則です。つまり熱力学第一法則は、孤立系の内部エネルギーは一定であるということができます。
Sponsored Link
Sponsored Link
定容熱容量と定圧熱容量
物質の温度を1℃(1K)上昇させるのに必要な熱量を熱容量と言います。さらに物質1gあたりに換算した熱容量を比熱容量と言います。熱容量には以下の2つがあります。
- 定容熱容量;体積を一定にしたときの熱容量
- 定圧熱容量;圧力を一定にしたときの熱容量
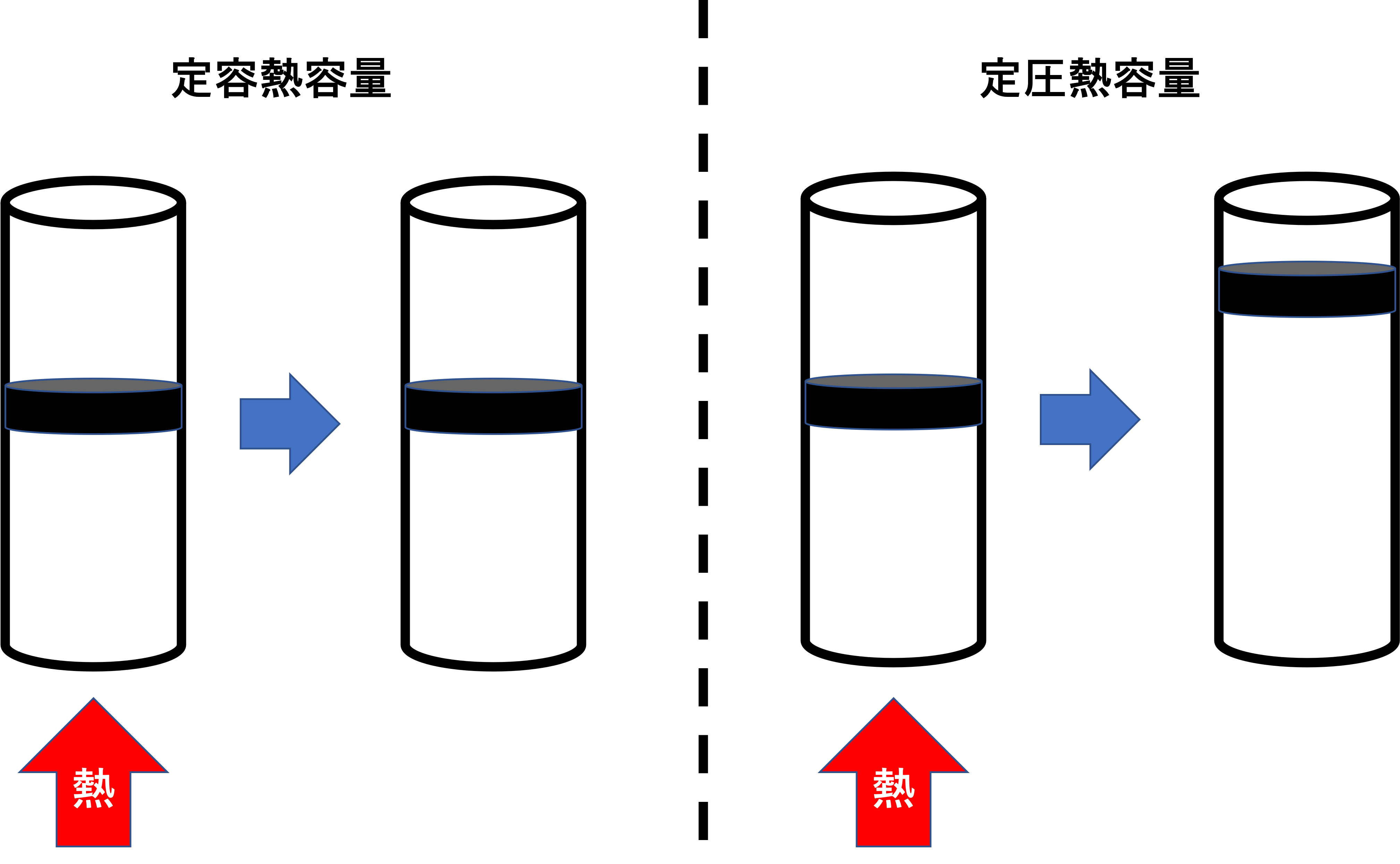
定圧の場合、熱を加えると圧力を一定に保とうとして、体積が変わります。つまりピストンの移動が起こり仕事が行われ、その分余計な熱を消費します。
それに対して定容の場合は、体積が一定であるためピストンの移動がなく仕事が行われません。よって定容の時は先ほどのような無駄な熱を消費しません。
このことから、定容の場合に比べて定圧の方が物質の温度を上昇させるのにより熱を必要とするため、定容熱容量<定圧熱容量となります。
まとめ
- 運動エネルギーと位置エネルギーの総和を内部エネルギーと言う。
- 孤立系の内部エネルギーが一定であることを熱力学第一法則と言う。
- 定容熱容量<定圧熱容量となる。
