

Sponsored Link
製剤、輸液の電解質の単位mEq/Lとは?計算方法は?
輸液の袋を良く見てみると、ナトリウムやカリウムの電解質や、浸透圧が記載されています。今回は、電解質の計算などについて見ていきたいと思います。
当量濃度
当量濃度は、輸液などの溶液にどれくらい電解質が入っているかを表す単位です。一般的に、mEq/Lで表され、「メックパーリットル」と読みます。まずmEq/Lの存在意義について見てみます。
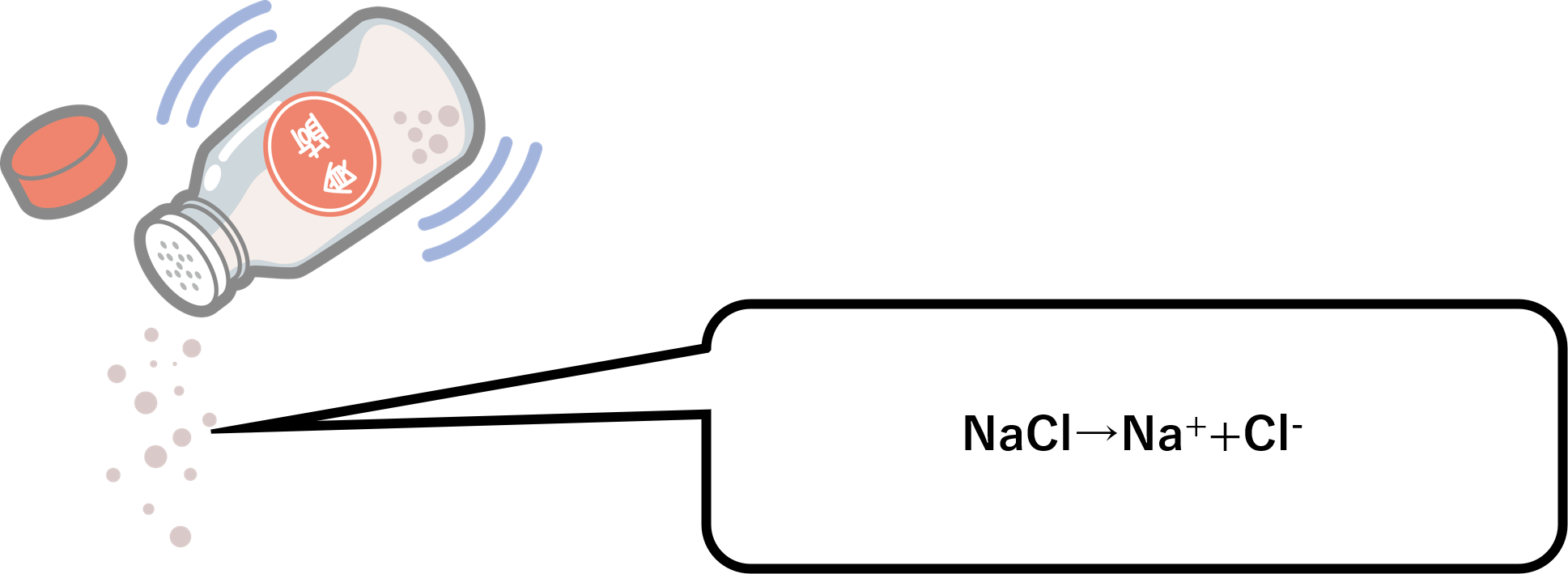
例えば、塩化ナトリウムNaCl9gを水1Lに溶かすと、
NaCl→Na++Cl-(見にくくてすいません)と解離します。細かい計算は割愛しますが、これをg/Lで表すとなると、
- Na+;3.54g/L
- Cl-;5.46g/L
となってしまい、陽イオンと陰イオンのバランスが取れているかわかりません。
しかし、mEq/Lで表すと、
- Na+;154mEq/L
- Cl-;154mEq/L
となり、プラスとマイナスのバランスが取れていることがわかります。このように電解質のバランスを見るにはmEq/Lの方がわかりやすいのです。存在意義を確認してもらったところで、どうやって154mEq/Lを出したのか確認していきましょう。
Sponsored Link
Sponsored Link
NaClのmEq/L計算
まずNaの原子量が23、Clの原子量が35.5であるため、NaClは58.5となります。今回はNaCl9gを溶かすため、9/58.5=0.154mol溶かすことになります。
これを1Lの水溶かしているため、0.154mol/Lとなります。これに1/1000を表すm(ミリ)をつけて換算すると、154mmol/Lとなります。
Eqはequivalent(当量)の略で、それの1/1000がmEqです。mEq/Lは溶液1Lに溶けている溶質の当量数を表します。そのため、mEq/L=mmol/L×電荷数で表すことができます。
ここでNaClの反応式に戻ると、Na+とCl-に解離するため、Na+とCl-の電荷数はそれぞれ1です。そして、それぞれ154mmol/Lあります。よって掛け算して
- Na+;154mEq/L
- Cl-;154mEq/L
となったのです。では例題を解いて見ましょう。
例題
カリウム値が低下したため、15%塩化カリウム(KCl)注射液20mlを5%ブドウ糖液500mlに混合したものを1回分として、1日2回点滴静注した。これによって供給される1日のカリウムは何mEqか?
ただし、原子量はK39、Cl35.5とする。
15%塩化カリウム注射液は、15%であるため、1ml中に0.15gの塩化カリウムを含みます。そのため、20mlを1日2回であるため、KClは0.15×20×2=6gが総量となります。
KClの分子量は74.5であるため、6/74.5=0.08molとなります。これが500mlのブドウ糖2本に溶かされるわけですから、0.08mol/Lとなります。これをmmol/Lに換算すると、80mmol/Lとなります。
KCl→K++Cl-となるため、カリウムの電荷数は1となります。
よって答えは80mEq/Lとなります。
まとめ
- 電解質のバランスを見るにはmEq/Lがわかりやすい。
- mEq/L=mmol/L×電荷数
